Radioactiviteit
Alle stoffen zijn opgebouwd uit atomen, en elk atoom bestaat uit een atoomkern en elektronen. Niet alle atoomkernen zijn echter stabiel. Wanneer de atoomkern verandert spreken we van radioactief verval. Daarbij komt ioniserende straling vrij: alfa-, bèta- of gammastraling.
Isotopen
Een atoomkern bestaat uit protonen en neutronen. Het aantal protonen bepaalt welke atoomsoort het is, het aantal neutronen kan verschillen. Een atoomsoort kan dus verschillende isotopen hebben: isotopen hebben hetzelfde aantal protonen maar een verschillend aantal neutronen in de kern.
Isotopen worden beschreven aan de hand van het atoomnummer en het massagetal:
- Het atoomnummer geeft aan hoeveel protonen er in de kern van het atoom zitten, en bepaalt dus de atoomsoort. Je kunt het atoomnummer van elke atoomsoort vinden in het periodiek systeem (in bijvoorbeeld een tabellenboek).
- Het massagetal is het totaal aantal deeltjes, dus protonen plus neutronen, in de kern.
Hieronder staan verschillende manieren om de naam van een isotoop op te schrijven. Een ijzer-56-kern heeft dus 26 protonen en (56-26=) 30 neutronen.
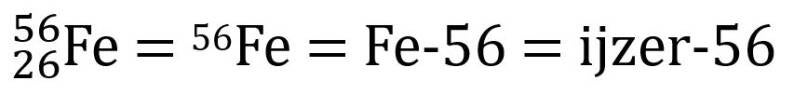
In de volgende afbeelding staat een lithium-7-atoom schematisch weergegeven. Lithium heeft atoomnummer 3, dus 3 protonen in de kern. Daarnaast zitten in de kern (7-3=) 4 neutronen.
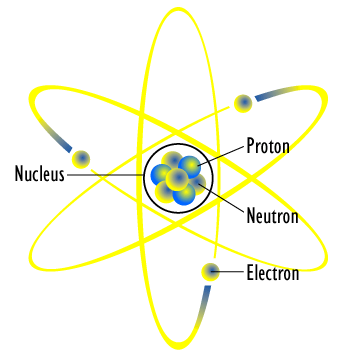
Schematische weergave van een lithium-7-atoom.
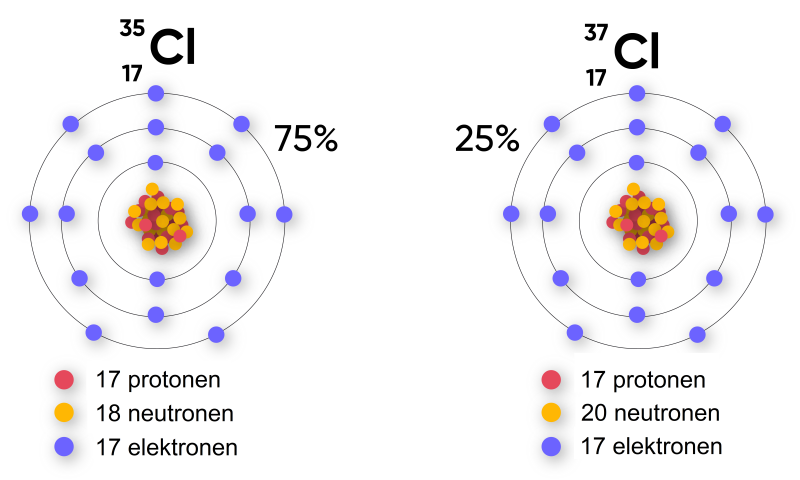
In de natuur komen er twee verschillende stabiele isotopen van chloor voor.
Van dezelfde atoomsoort kunnen er dus meerdere isotopen zijn. Zo heeft chloor 2 verschillende stabiele isotopen die in de natuur bestaan: chloor-35 en chloor-37. Er zijn echter ook isotopen van chloor die niet stabiel zijn, bijvoorbeeld chloor-34, chloor-36, chloor-38 en chloor-39. Dit zijn radioactieve isotopen, die na verloop van tijd uit elkaar vallen en daarbij ioniserende straling uitzenden.
Ioniserende straling
De straling die vrijkomt bij radioactief verval is ioniserend: wanneer het tegen een atoom botst kan het atoom geïoniseerd worden. Dit betekent dat er elektronen losgemaakt worden, het atoom wordt dan een ion. Moleculen worden dan beschadigd. Voor mensen kan dit schadelijk zijn: wanneer DNA-moleculen beschadigd raken kunnen lichaamscellen veranderen. Wanneer de hoeveelheid ioniserende straling te groot is en het lichaam niet in staat is dit snel genoeg te herstellen kan dit ernstige ziektes veroorzaken.
Er zijn vele soorten ioniserende straling, de bekendste zijn alfastraling, bètastraling en gammastraling.
Alfastraling
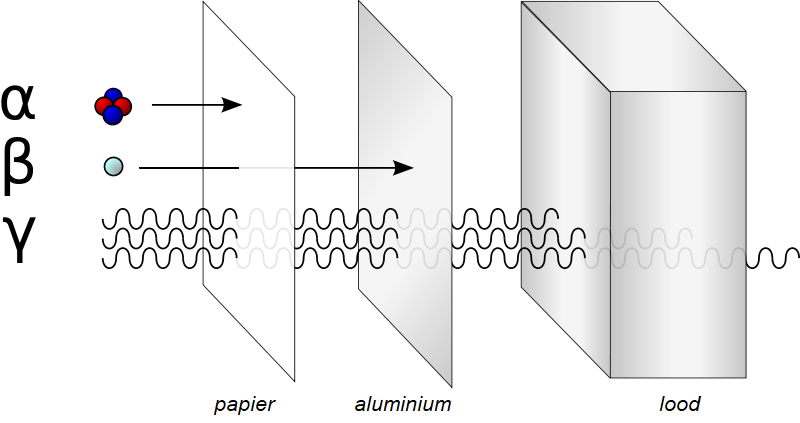
Bij alfastraling (aangegeven met de Griekse letter α) wordt er een α-deeltje uitgezonden. Dat deeltje bestaat uit twee protonen en twee neutronen, die loskomen uit de atoomkern. De atoomkern verandert hierdoor dus! Een α-deeltje is, relatief gezien, een groot en zwaar deeltje. Hierdoor kan hij bij een botsing veel schade aanrichten. Alfastraling heeft wel een zeer klein doordringend vermogen: een paar centimeter lucht of een velletje papier zijn al genoeg om α-deeltjes tegen te houden.

Bètastraling
Bij bètastraling (aangegeven met de Griekse letter β) wordt er een β-deeltje uitgezonden. Dat deeltje is een elektron die de atoomkern verlaat. Dit elektron is ontstaan omdat een neutron in de kern veranderde in een proton en een elektron. De atoomkern verandert hierdoor dus! Een β-deeltje is véél kleiner en lichter dan een α-deeltje. Bètastraling heeft daardoor een groter doordringend vermogen. Voor het tegenhouden van β-deeltjes heb je bijvoorbeeld een metalen plaatje of een dik boek nodig.
Doordringend vermogen van alfa-, bèta- en gammastraling.
Halveringstijd
Bij alfa- en bètastraling verandert de atoomkern die de deeltjes uitzendt: het wordt een andere isotoop. Hierdoor neemt het aantal kernen van de radioactieve isotoop in de stof dus af. Hoe snel dat gebeurt is afhankelijk van de halveringstijd. De halveringstijd (symbool: t1/2) geeft aan hoe lang het gemiddeld duurt totdat nog maar de helft van het oorspronkelijke aantal kernen over is. De halveringstijden van isotopen verschillen enorm: polonium-214 heeft bijvoorbeeld een halveringstijd van 0,2 milliseconde, terwijl uranium-238 een halveringstijd van een miljard jaar heeft. Je kunt deze halveringstijden opzoeken in een tabel.
Om te laten zien hoe halveringstijd werkt gebruiken we als voorbeeld het isotoop natrium-24. Deze heeft een halveringstijd van 15,0 uur. Stel, je begint met 1 000 000 natrium-24-kernen, dan zijn er na 15,0 uur dus 500 000 over. Wanneer je dan nog een keer 15,0 uur verder gaat, is het aantal weer gehalveerd. Er zijn dan nog 250 000 kernen over. Na nog een keer 15,0 uur (dus na in totaal 45,0 uur) zijn er nog 125 000 natrium-24-kernen. Nog een halveringstijd verder, dus na in totaal 60,0 uur, heb je nog 62 500 natrium-24-kernen. Enzovoorts!
Gammastraling
Gammastraling bestaat niet (zoals alfa- en bètastraling) uit deeltjes, maar is een elektromagnetische golf. Het is een bundeltje energie die uitgezonden wordt als de atoomkern van een hogere naar een lagere energietoestand gaat. De samenstelling van de atoomkern, en daarmee de isotoop die je hebt, verandert daarbij niet. De golflengte van gammastraling is heel klein, waardoor de straling ook door vaste stoffen heen kan. Het heeft dus een groot doordringend vermogen.
Halveringsdikte
Gammastraling wordt door stoffen niet tegengehouden, maar de hoeveelheid straling wordt wel minder hoe dikker het materiaal is waar de straling doorheen gaat. Hoe goed een materiaal de hoeveelheid gammastraling kan verminderen is afhankelijk van de halveringsdikte. De halveringsdikte (symbool: d1/2) geeft aan hoeveel centimeter materiaal je nodig hebt om de hoeveelheid straling te halveren.
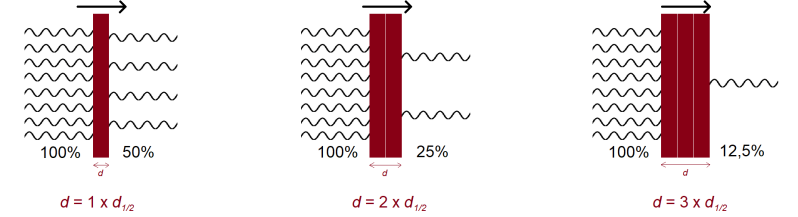
Een voorbeeld: aluminium heeft (voor zachte gammastraling) een halveringsdikte van 6,0 cm. Dit betekent dat je een aluminiumplaat van 6,0 cm dik nodig hebt om nog maar 50% van de oorspronkelijke hoeveelheid straling over te houden. Wanneer je plaat 12,0 cm (dus twee halveringsdiktes) dik is halveert de hoeveelheid straling nog een keer, en heb je nog maar 25% van de straling over. Met een 18,0 cm dikke plaat nog 12,5%, enzovoorts.
Halveringsdikte: elke keer als er een halveringsdikte bij komt, wordt de hoeveelheid doorgelaten straling gehalveerd.
Stralingsbronnen
Overal waar je bent is er ioniserende straling, we noemen dit de achtergrondstraling. Deze is voor een groot deel afkomstig van radioactieve isotopen in natuurlijke materialen in de grond, en daardoor ook in bouwmaterialen. Een ander deel van de achtergrondstraling is afkomstig uit de ruimte, vanuit andere sterrenstelsels, onze atmosfeer beschermt ons daar voor het grootste deel tegen. De totale hoeveelheid achtergrondstraling is zo klein, dat je je er geen zorgen om hoeft te maken. In het vliegtuig, op zo'n 10 km hoogte, is de achtergrondstraling een stuk groter, maar ook dat blijft ver onder de veilige grenswaarde.
Ioniserende straling komt ook van niet-natuurlijk bronnen. Hiervoor moeten radioactieve isotopen gemaakt worden. Dit gebeurt vooral in de nucleaire industrie: in een kerncentrale blijven veel verschillende soorten radioactieve isotopen als afval over. Omdat een deel ervan een zeer grote halveringstijd heeft blijven deze isotopen een lange tijd straling uitzenden. Daarom moet er voorkomen worden dat deze isotopen vrij in de natuur komen, en moet het voor lange tijd veilig opgeslagen worden.

Al het Nederlandse kernafval wordt opgeslagen bij het COVRA in Borsele.

Radioactieve isotopen worden opgeslagen in vaten met dikke betonnen wanden.
Toepassingen in de medische wereld
Ioniserende straling is niet alleen schadelijk, maar wordt ook nuttig toegepast, bijvoorbeeld in de medische wereld. Dit gebeurt zowel bij het stellen van diagnoses als bij de behandeling van, vooral, tumoren.
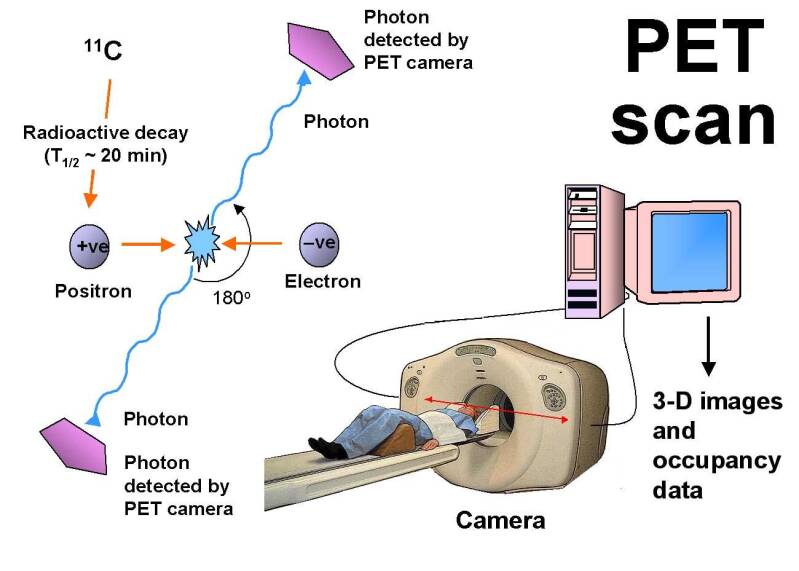
In de medische beeldvorming worden, in zeer kleine hoeveelheden, radioactieve isotopen gebruikt om een diagnose te kunnen stellen. Er wordt dan een tracer ingebracht: een radioactief isotoop die op een bepaalde plek of in ene bepaald orgaan net zo goed opgenomen wordt als het niet-radioactieve isotoop van dezelfde stof. Doordat het radioactieve isotoop gammastraling uitzendt kan met detectoren de locatie van het isotoop in beeld gebracht worden, en wanneer je het een tijdje volgt krijg je informatie over het functioneren van een orgaan of deel van het lichaam. Dit is de techniek die bijvoorbeeld in PET-scans en SPECT-scans gebruikt wordt.
In grotere dosissen kunnen radioactieve isotopen ook gebruikt worden om tumoren te behandelen. De bedoeling is dan dat zo precies mogelijk de tumor bestraald wordt, zodat de juiste cellen stuk gemaakt worden. Daar zijn verschillende manieren voor. Men doet dit vanuit een externe bron (vaak met gammastraling die heel precies gericht wordt), of men kan radioactieve isotopen (vaak bètastralers) in het lichaam plaatsen, zo dicht mogelijk tegen of zelfs in de tumor.
De isotopen die in onze gezondheidszorg gebruikt worden worden geproduceerd in een kleine kerncentrale of in een cyclotron. De centrale in het Noord-Hollandse Petten verzorgt ongeveer 30% van de wereldwijde productie van radioactieve isotopen voor medisch gebruik.